Høringsinnspill - lov og forskrift om EU forordningen om medisinsk og in vitro-diagnostisk medisinsk utstyr
Høringsinnspill - lov og forskrift om medisinsk utstyr for å gjennomføre forordning (EU) 2017/745 om medisinsk og forordning (EU) 2017/746 om in vitro-diagnostisk medisinsk utstyr.
Norsk radiografforbund organiserer radiografer og stråleterapeuter. Våre medlemmer arbeider for en stor del innen bildediagnostikk i spesialisthelsetjenesten og ved private institutter som tilbyr bildediagnostikk. Vi organiserer også en del medlemmer blant utstyrsleverandører av medisinsk teknisk utstyr samt leverandører av legemidler brukt innen bildediagnostikk.
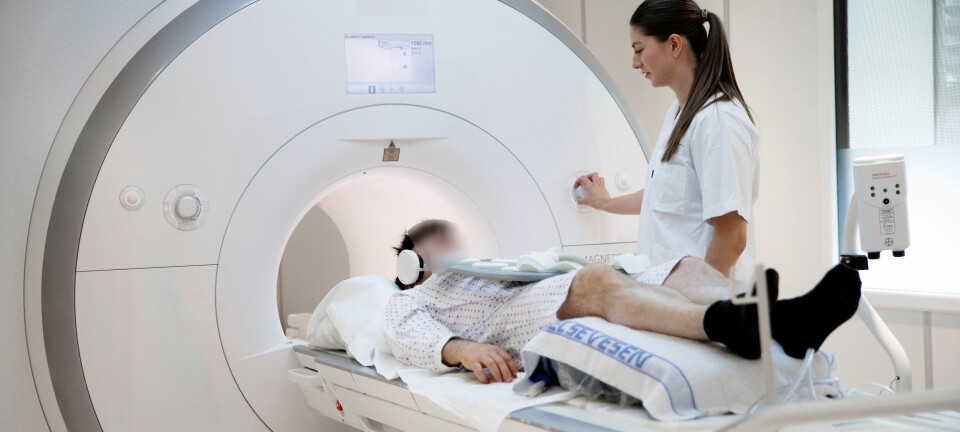
Register over MTUEt register over alt av medisinsk utstyr som inkluderer elektroniske implantater bør også ha en oversikt over MR-kompatibilitet til utstyr som er listet. Bildediagnostikk med bruk av MR gjør bruk av sterke oscillerende magnetfelt. Oscillerende magnetfelt vil kunne indusere tilleggsstrøm i elektroniske implantat. En MR undersøkelse vil derfor kunne skade/ødelegge funksjon av elektroniske implantater som i verste fall kan skade pasient.
Et mye brukt implantat som kan nevnes er pacemakere. Før en MR undersøkelsene er pacemakere et sentralt implantat å kartlegge. Pacemakere finnes implantert i pasienter både som MR kompatible og inkompatible. En utvikling mot stadig sterkere magnetfelt i klinisk bruk av MR medfører at flere implantater som tidligere har vært regnet som kompatible, nå ofte må regnes som inkompatible, alt etter styrken på magnetfeltet.Kartlegging av slike implantater forut for en MR undesøkelse er en daglig utfordring for radiografer og radiologer i bildediagnostikken. Det er ofte vanskelig, noen ganger umulig, å finne fram til informasjon om beskaffenheten til slike implantert i pasientene. Resultatet er ikke sjelden at viktige MR undersøkelser avlyses, med det resultat at pasientene kan få mindre presis bildediagnostikk i sin utredning.Det er forventet videre utvikling mot økt bruk av ulike elektroniske implantater i pasienter.Viser også til vedlagt lenke til læringsnotat fra Helsedirektoratet i 2017.https://www.helsedirektoratet.no/laeringsnotat/bruk-av-mr-sjekkliste/Bruk%20av%20MR-sjekkliste.pdf/_/attachment/inline/226b04a3-f93e-4c56-95fc-619bf7447d2c:4fbdda5986f3c8fb6e4bf5b521e47856b73d0c4b/Bruk%20av%20MR-sjekkliste.pdfTilsynsmyndigheterFor oss virker det litt uklart hvordan samspillet mellom flere ulike tilsynsmyndigheter i fremtiden skal foregå. En kan stå i fare for at tilsynsfunksjonene fragmenteres. Noen spørsmål vi har stilt oss er: Hvordan skal strålevernets (DSA) rolle være i forhold til legemiddelverket.
Skal de regulere hver sin type utstyr. Hva med programvare i røntgenmodaliteter, programvare som oppgradering med jevne mellomrom.Videre arbeid mot bedre oversikt på dette feltetI det videre arbeidet med dette feltet bør en legge til rette for nasjonale register som inkluderer oversikt over elektroniske implantat i pasienter.Informasjon i slike registre bør i fremtiden være lett tilgjengelig for helsepersonell med rekvisisjonsrett til bildediagnostikk. Slik informasjon bør også være tilgjengelig for radiologer og radiografer samt stråleterapeuter ved vurdering og prioritering til bildediagnostikk.